Probióticos y Síndrome del Intestino Irritable: La Guía Definitiva Basada en la Ciencia para Encontrar Alivio
¿Sufres de Síndrome del Intestino Irritable? Analizamos a fondo múltiples meta-análisis con más de 9.000 pacientes para revelarte qué probióticos funcionan realmente, para qué síntomas, en qué dosis, y qué otros tratamientos coadyuvantes como la dieta baja en FODMAPs pueden transformar tu salud intestinal.
SINDROME DEL INTESTINO IRRITABLE
Nuri El azem De haro
10/3/20258 min leer

Probióticos y Síndrome del Intestino Irritable: La Guía Definitiva Basada en la Ciencia para Encontrar Alivio
El Síndrome del Intestino Irritable (SII) es mucho más que un simple "dolor de estómago". Es un trastorno gastrointestinal crónico y complejo que afecta a entre el 5% y el 10% de la población mundial, con una prevalencia mayor en mujeres [5]. Se caracteriza por un conjunto de síntomas debilitantes: dolor abdominal recurrente, hinchazón, gases y una alteración persistente de los hábitos intestinales, ya sea en forma de diarrea (SII-D), estreñimiento (SII-E) o una mezcla de ambos (SII-M) [1, 5]. Además del malestar físico, el SII impone una carga económica y social sustancial, afectando gravemente la calidad de vida y la productividad de quienes lo padecen [3, 6].
Durante mucho tiempo, los tratamientos se han centrado en aliviar los síntomas de forma aislada. Sin embargo, un creciente cuerpo de evidencia científica ha desplazado el foco hacia un ecosistema complejo y fascinante: la microbiota intestinal. La idea de que un desequilibrio en nuestras bacterias intestinales es una pieza central en el rompecabezas del SII ha ganado una fuerza inmensa [3]. Esto nos lleva a una pregunta crucial: ¿pueden los probióticos, los "microorganismos vivos beneficiosos", ser la clave para un alivio real y sostenido?
Para responder a esta pregunta, hemos analizado en profundidad seis revisiones sistemáticas y meta-análisis de gran envergadura, que en conjunto evalúan los datos de decenas de ensayos clínicos y miles de pacientes. Este es el veredicto de la ciencia.
El Origen del Problema: ¿Qué Causa el Síndrome del Intestino Irritable?
El SII se entiende hoy como un trastorno de la interacción cerebro-intestino [3, 6]. No es una enfermedad imaginaria; es una condición real con bases fisiopatológicas complejas. Las principales teorías científicas apuntan a:
Disbiosis Intestinal: Es la alteración del equilibrio de la microbiota intestinal. Los pacientes con SII a menudo presentan una menor diversidad de microorganismos y una reducción de bacterias beneficiosas clave, como Bifidobacterium y Lactobacillus, mientras que aumentan otras familias potencialmente pro-inflamatorias como Enterobacteriaceae [1, 5].
Inflamación de Bajo Grado y Permeabilidad Intestinal: Se ha observado un aumento de la permeabilidad de la barrera intestinal (el llamado "intestino permeable") en pacientes con SII. Esto permite que ciertas sustancias pasen al torrente sanguíneo, activando el sistema inmunitario de la mucosa y generando una inflamación leve pero crónica que contribuye a los síntomas [1, 5].
Hipersensibilidad Visceral: Los nervios del intestino de las personas con SII son hipersensibles. Esto significa que reaccionan de forma exagerada a estímulos normales, como la distensión por gas o los movimientos intestinales, interpretándolos como dolor intenso [1, 5].
Alteración de los Ácidos Grasos de Cadena Corta (AGCC): Estos compuestos (acetato, propionato y butirato) son producidos por la microbiota al fermentar la fibra y son vitales para la salud del colon. Los estudios muestran un perfil alterado de AGCC en pacientes con SII, destacando un aumento significativo de propionato y una reducción en la proporción de acetato, lo que podría servir como biomarcador de la enfermedad [7].
Dado que la microbiota está implicada en todos estos procesos, la modulación de su composición y actividad a través de probióticos se presenta como una estrategia terapéutica directa y prometedora [3].
La Evidencia Científica: ¿Qué nos Dicen los Grandes Estudios?
Para evaluar la eficacia de los probióticos, no podemos basarnos en un solo estudio. La evidencia más sólida proviene de los meta-análisis, que son estudios estadísticos que combinan los resultados de múltiples ensayos clínicos controlados y aleatorizados (ECA). Los artículos analizados para esta guía agrupan datos de hasta 81 ECA y más de 9.200 participantes, ofreciendo una perspectiva muy robusta [3, 6].
El consenso abrumador de estos análisis es claro: los probióticos, como categoría general, son significativamente más eficaces que el placebo para mejorar los síntomas globales del SII, el dolor abdominal y la calidad de vida de los pacientes [1, 4, 5, 6]. Un meta-análisis de tres niveles, un método estadístico avanzado, estimó que los probióticos tienen un tamaño de efecto de mediano a grande en la mejora de estos síntomas [6].
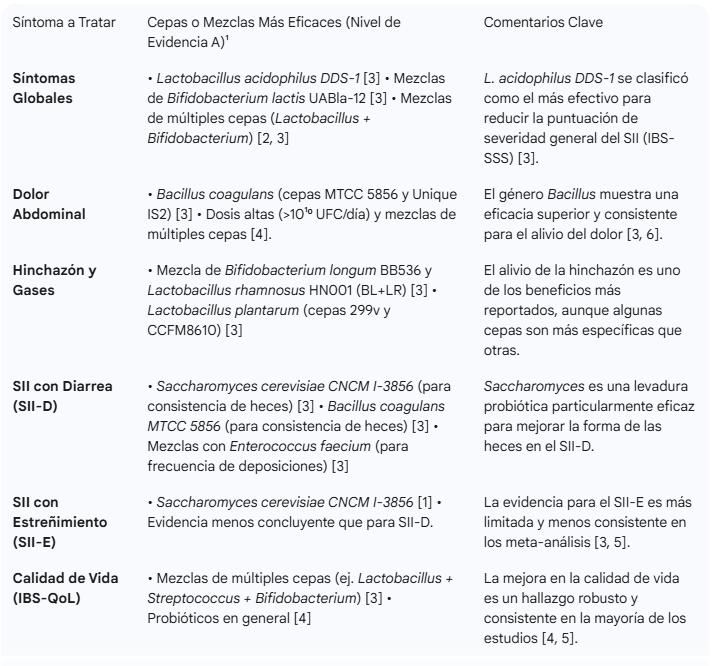
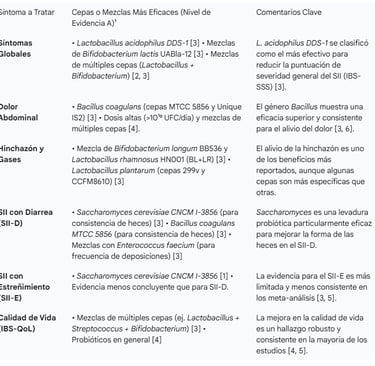
La Clave Está en la Cepa: Guía de Probióticos para Cada Síntoma
La pregunta más importante no es si los probióticos funcionan, sino cuáles funcionan y para qué. Gracias a los meta-análisis en red, que comparan múltiples tratamientos simultáneamente, podemos clasificar la eficacia de cepas y mezclas específicas para cada síntoma.
Tabla de Eficacia de Probióticos en el SII (Basada en Meta-Análisis en Red)
¹ El Nivel de Evidencia A se refiere a probióticos que no solo son superiores al placebo, sino también a otros probióticos con eficacia demostrada [3].
Esta tabla es muy importante, porque según el problema que presente cada paciente, podremos seleccionar la mejor cepa para tratarnos según nuestros síntomas. Por ello, si queréirs buscar un producto acorde a vuestras necesidades,os dejo un enlace a la pagina de Amazon:
Dosis y Duración: ¿Cuánto y por Cuánto Tiempo?
Dosis: La mayoría de los estudios respaldan una dosis mínima de 10⁹ UFC (mil millones de unidades formadoras de colonias) al día para observar efectos [1]. Para síntomas más específicos como el dolor abdominal, dosis más altas, superiores a 10¹⁰ UFC/día, parecen ofrecer un mayor beneficio [4].
Duración: Los efectos beneficiosos de los probióticos pueden comenzar a notarse a las 4 semanas de tratamiento continuo [1]. Curiosamente, un meta-análisis de gran escala observó que los tratamientos de duración más corta (menos de 4 semanas) se asociaban con un mayor tamaño del efecto, mientras que los efectos tendían a disminuir en estudios más largos [6]. Esto no invalida los tratamientos a largo plazo, pero sugiere que el beneficio inicial puede ser el más pronunciado, posiblemente debido a un fuerte efecto placebo en las primeras semanas o a la inclusión de pacientes con síntomas más severos en estudios más largos [6].
Tratamientos Coadyuvantes: Potenciando los Resultados
Tomar probióticos es solo una parte de la estrategia. Para un manejo integral del SII, es fundamental considerar otros enfoques que actúan en sinergia.
La Dieta Baja en FODMAPs: El Coadyuvante Estrella
La dieta baja en FODMAPs (Oligosacáridos, Disacáridos, Monosacáridos y Polioles Fermentables) es una de las intervenciones dietéticas con mayor respaldo científico para el SII [2]. Estos carbohidratos de cadena corta son mal absorbidos en el intestino delgado y fermentados rápidamente por las bacterias, produciendo gas y atrayendo agua, lo que causa hinchazón, dolor y diarrea [7].
Eficacia: Los meta-análisis confirman que una dieta baja en FODMAPs es altamente eficaz para mejorar los síntomas globales y reducir la severidad del SII [2, 7].
Sinergia con Probióticos: La combinación de una dieta baja en FODMAPs junto con la suplementación con probióticos ha demostrado ser la estrategia más efectiva de todas para el alivio de los síntomas del SII en algunos estudios [2]. Mientras la dieta reduce el "combustible" para las bacterias productoras de gas, los probióticos ayudan a restaurar un equilibrio más saludable.
Efecto sobre los AGCC: Una dieta baja en FODMAPs ha demostrado reducir significativamente las concentraciones fecales de propionato, el cual se encuentra elevado en pacientes con SII, ayudando a normalizar el perfil de metabolitos intestinales [7].
Otras Intervenciones: Prebióticos, Simbióticos y Trasplante Fecal
Prebióticos y Simbióticos: A diferencia de los probióticos, la evidencia actual sobre los prebióticos (fibra que alimenta a las bacterias buenas) y los simbióticos (combinación de prebióticos y probióticos) es débil e inconsistente. Los meta-análisis no han encontrado un beneficio significativo de estas intervenciones sobre el placebo para el SII [1, 5].
Trasplante de Microbiota Fecal (TMF): Este procedimiento consiste en transferir la microbiota de un donante sano al intestino del paciente. El meta-análisis en red muestra que el TMF es una opción terapéutica eficaz, con una efectividad comparable a la de los probióticos [5]. Aunque es más invasivo, representa una alternativa prometedora, especialmente para casos más resistentes.
Una Mirada Crítica: Fortalezas, Debilidades y Puntos en Común
Fortalezas Comunes:
Consenso sobre la Eficacia: Todos los meta-análisis concluyen que los probióticos son superiores al placebo.
Seguridad: Los probióticos son extremadamente seguros. El número de eventos adversos no es significativamente diferente al del grupo placebo [1, 4, 5].
Personalización: La evidencia apunta a un futuro de tratamiento personalizado, seleccionando cepas específicas para los síntomas predominantes de cada paciente [3]
Debilidades y Desafíos:
Heterogeneidad: Es el principal "punto débil". Los estudios analizados son muy diferentes entre sí (cepas, dosis, duración, poblaciones), lo que dificulta extraer conclusiones definitivas para una única formulación [3, 6].
Falta de Comparaciones Directas: La mayoría de los ensayos comparan un probiótico con un placebo, no entre sí. Se necesitan más estudios "cara a cara" [3].
Efectos a Largo Plazo: La mayoría de los estudios son a corto plazo. Se necesita más investigación sobre la sostenibilidad de los beneficios y la necesidad de un tratamiento continuo [6].
Conclusiones Prácticas: Tu Hoja de Ruta para Manejar el SII
Los Probióticos son una Terapia Válida y Eficaz: No son un remedio milagroso, pero sí una herramienta terapéutica con un sólido respaldo científico para el SII [1, 2, 3, 4, 5, 6].
Identifica tu Síntoma Dominante para Elegir la Cepa: No todos los probióticos sirven para todo. Utiliza la tabla de este artículo como una guía inicial para buscar productos que contengan las cepas más estudiadas para tu problema principal (dolor, hinchazón, diarrea) [3].
Verifica la Dosis: Busca productos que garanticen una dosis de al menos 10⁹ UFC/día [1].
Combina con la Dieta Baja en FODMAPs: Esta combinación ha demostrado ser la estrategia más potente. Considera trabajar con un dietista-nutricionista para implementar esta dieta de forma correcta, ya que es restrictiva y debe ser supervisada [2, 7].
Sé Consistente y Paciente: Da al tratamiento un mínimo de 4 semanas para evaluar su eficacia [1]. Los cambios en la microbiota y la respuesta sintomática no son inmediatos.
Consulta Siempre a un Profesional de la Salud: Este artículo es informativo, pero no reemplaza el consejo médico. Habla con tu médico o gastroenterólogo antes de iniciar cualquier nuevo tratamiento para asegurar que es la opción adecuada para ti.
En resumen, la ciencia nos dice que modular nuestra microbiota intestinal es una de las estrategias más efectivas que tenemos para manejar el Síndrome del Intestino Irritable. Los probióticos, seleccionados de forma inteligente y combinados con enfoques dietéticos como la dieta baja en FODMAPs, ofrecen una esperanza real y tangible para recuperar la calidad de vida que esta condición a menudo nos arrebata.
Bibliografía
[1] Zhang, W. X., Shi, L. B., Zhou, M. S., Wu, J., & Shi, H. Y. (2023). Efficacy of probiotics, prebiotics and synbiotics in irritable bowel syndrome: a systematic review and meta-analysis of randomized, double-blind, placebo-controlled trials. Journal of Medical Microbiology, 72(10), 001758. (jmm001758.pdf)
[2] Lei, Y., Sun, X., Ruan, T., Lu, W., Deng, B., Zhou, R., & Mu, D. (2025). Effects of Probiotics and Diet Management in Patients With Irritable Bowel Syndrome: A Systematic Review and Network Meta-analysis. Nutrition Reviews, 83(9), 1743–1756. (nuae217.pdf)
[3] Xie, P., Luo, M., Deng, X., Fan, J., & Xiong, L. (2023). Outcome-Specific Efficacy of Different Probiotic Strains and Mixtures in Irritable Bowel Syndrome: A Systematic Review and Network Meta-Analysis. Nutrients, 15(17), 3856. (nutrients-15-03856.pdf)
[4] Yang, R., Jiang, J., Ouyang, J., Zhao, Y., & Xi, B. (2024). Efficacy and safety of probiotics in irritable bowel syndrome: A systematic review and meta-analysis. Clinical Nutrition ESPEN, 60, 362-372. (1-s2.0-S2405457724000494-main.pdf)
[5] Wu, Y., Li, Y., Zheng, Q., & Li, L. (2024). The Efficacy of Probiotics, Prebiotics, Synbiotics, and Fecal Microbiota Transplantation in Irritable Bowel Syndrome: A Systematic Review and Network Meta-Analysis. Nutrients, 16(13), 2114. (nutrients-16-02114.pdf)
[6] Chen, M., Yuan, L., Xie, C. R., Wang, X. Y., Feng, S. J., Xiao, X. Y., & Zheng, H. (2023). Probiotics for the management of irritable bowel syndrome: a systematic review and three-level meta-analysis. International Journal of Surgery, 109(10), 3631–3647. (js9-109-3631.pdf)
[7] Ju, X., Jiang, Z., Ma, J., & Yang, D. (2024). Changes in Fecal Short-Chain Fatty Acids in IBS Patients and Effects of Different Interventions: A Systematic Review and Meta-Analysis. Nutrients, 16(11), 1727. (nutrients-16-01727.pdf)